Фосфорная кислота сильный или слабый электролит. Сильные и слабые электролиты. Степень электролитической диссоциации
, , 21 , , ,
, 25-26 , 27-28 ,
, 30, , , , , , , , /2003
§ 6.3. Сильные и слабые электролиты
Материал этого раздела частично вам знаком по ранее изученным школьным курсам химии и из предыдущего раздела. Кратко повторим, что вам известно, и познакомимся с новым материалом.
В предыдущем разделе мы обсуждали поведение в
водных растворах некоторых солей и органических
веществ, полностью распадающихся на ионы в
водном растворе.
Имеется ряд простых, но несомненных
доказательств того, что некоторые вещества в
водных растворах распадаются на частицы. Так,
водные растворы серной H 2 SO 4 , азотной HNO 3 ,
хлорной HClO 4 , хлороводородной (соляной) HCl,
уксусной CH 3 COOH и других кислот имеют кислый
вкус. В формулах кислот общей частицей является
атом водорода, и можно предположить, что он (в
виде иона) является причиной одинакового вкуса
всех этих столь различных веществ.
Образующиеся при диссоциации в водном растворе
ионы водорода придают раствору кислый вкус,
поэтому такие вещества и названы кислотами. В
природе только ионы водорода имеют кислый вкус.
Они создают в водном растворе так называемую
кислотную (кислую) среду.
Запомните, когда вы говорите «хлороводород», то имеете в виду газообразное и кристаллическое состояние этого вещества, но для водного раствора следует говорить «раствор хлороводорода», «хлороводородная кислота» или использовать общепринятое название «соляная кислота», хотя состав вещества в любом состоянии выражается одной и той же формулой – НСl.
Водные растворы гидроксидов лития (LiOH), натрия
(NаОН), калия (КОН), бария (Ва(ОН) 2), кальция
(Са(ОН) 2) и других металлов имеют одинаковый
неприятный горько-мыльный вкус и вызывают на
коже рук ощущение скольжения. По-видимому, за это
свойство ответственны гидроксид-ионы ОН – ,
входящие в состав таких соединений.
Хлороводородная HCl, бромоводородная HBr и
йодоводородная HI кислоты реагируют с цинком
одинаково, несмотря на свой различный состав, т.
к. в действительности с цинком реагирует не
кислота:
Zn + 2НСl = ZnСl 2 + Н2,
а ионы водорода:
Zn + 2H + = Zn 2+ + Н 2 ,
и образуются газообразный водород и ионы цинка.
Смешивание некоторых растворов солей, например
хлорида калия KCl и нитрата натрия NaNO 3 , не
сопровождается заметным тепловым эффектом, хотя
после выпаривания раствора образуется смесь
кристаллов четырех веществ: исходных – хлорида
калия и нитрата натрия – и новых – нитрата калия
КNO 3 и хлорида натрия NaCl. Можно предположить,
что в растворе две исходные соли полностью
распадаются на ионы, которые при его выпаривании
образуют четыре кристаллических вещества:
Сопоставляя эти сведения с
электропроводностью водных растворов кислот,
гидроксидов и солей и с рядом других положений,
С.А.Аррениус в 1887 г. выдвинул гипотезу
электролитической диссоциации, согласно которой
молекулы кислот, гидроксидов и солей при
растворении их в воде диссоциируют на ионы.
Изучение продуктов электролиза позволяет
приписать ионам положительные или отрицательные
заряды. Очевидно, если кислота, например азотная
НNO 3 , диссоциирует, предположим, на два иона
и при электролизе водного раствора на катоде
(отрицательно заряженный электрод) выделяется
водород, то, следовательно, в растворе имеются
положительно заряженные ионы водорода Н + .
Тогда уравнение диссоциации следует записать
так:
НNO 3 = Н + + .
Электролитическая диссоциация
–
полный или частичный распад соединения при его
растворении в воде на ионы в результате
взаимодействия с молекулой воды (или другого
растворителя).
Электролиты
– кислоты, основания или
соли, водные растворы которых проводят
электрический ток в результате диссоциации.
Вещества, не диссоциирующие в водном растворе на
ионы и растворы которых не проводят
электрический ток, называются неэлектролитами
.
Диссоциация электролитов количественно
характеризуется степенью диссоциации
– отношением числа распавшихся на ионы
«молекул» (формульных единиц) к общему числу
«молекул» растворенного вещества. Степень
диссоциации обозначается греческой буквой . Например, если из
каждых 100 «молекул» растворенного вещества 80
распадаются на ионы, то степень диссоциации
растворенного вещества равна: = 80/100 = 0,8, или 80%.
По способности к диссоциации (или, как говорят,
«по силе») электролиты разделяют на сильные
,
средние
и слабые
. По степени
диссоциации к сильным электролитам относят те из
них, для растворов которых > 30%, к слабым – < 3%, к средним – 3% 30%. Сила электролита –
величина, зависящая от концентрации вещества,
температуры, природы растворителя и др.
В случае водных растворов
к сильным электролитам
( > 30%) относят
перечисленные ниже группы соединений.
1
. Многие неорганические кислоты,
например хлороводородная НCl, азотная HNO 3 ,
серная H 2 SО 4 в разбавленных растворах.
Самая сильная неорганическая кислота – хлорная
НСlО 4 .
Сила некислородных кислот возрастает в ряду
однотипных соединений при переходе вниз по
подгруппе кислотообразующих элементов:
HCl – HBr – HI.
Фтороводородная (плавиковая) кислота HF растворяет стекло, но это вовсе не говорит о ее силе. Эта кислота из бескислородных галогенсодержащих относится к кислотам средней силы из-за высокой энергии связи Н–F, способности молекул HF к объединению (ассоциации) благодаря сильным водородным связям, взаимодействия ионов F – с молекулами НF (водородные связи) с образованием ионов и других более сложных частиц. В результате концентрация ионов водорода в водном растворе этой кислоты оказывается значительно пониженной, поэтому фтороводородную кислоту считают средней силы.
Фтороводород реагирует с диоксидом кремния, входящим в состав стекла, по уравнению:SiO 2 + 4HF = SiF 4 + 2H 2 O.
Фтороводородную кислоту нельзя хранить в стеклянных сосудах. Для этого используют сосуды из свинца, некоторых пластмасс и стекла, стенки которых покрыты изнутри толстым слоем парафина. Если для «травления» стекла использовать газообразный фтороводород, то поверхность стекла становится матовой, что используется для нанесения на стекло надписей и различных рисунков. «Травление» стекла водным раствором фтороводородной кислоты приводит к разъеданию поверхности стекла, которая остается прозрачной. В продаже обычно бывает 40%-й раствор плавиковой кислоты.
Сила однотипных кислородных кислот изменяется
в противоположном направлении, например йодная
кислота НIО 4 слабее хлорной кислоты НСlО 4 .
Если элемент образует несколько кислородных
кислот, то наибольшей силой обладает кислота, в
которой кислотообразующий элемент имеет самую
высокую валентность. Так, в ряду кислот НСlО
(хлорноватистая) – НСlО 2 (хлористая) – НСlО 3
(хлорноватая) – НСlО 4 (хлорная) последняя
наиболее сильная.
Один объем воды растворяет около двух объемов хлора. Хлор (примерно половина его) взаимодействует с водой:
Cl 2 + H 2 O = HCl + HСlO.
Хлороводородная кислота является сильной, в ее водном растворе практически нет молекул HCl. Правильнее уравнение реакции записать так:
Cl 2 + H 2 O = H + + Cl – + HClO – 25 кДж/моль.
Образующийся раствор называют хлорной водой.
Хлорноватистая кислота – быстродействующий окислитель, поэтому ее применяют для отбеливания тканей.
2 . Гидроксиды элементов главных подгрупп I и II групп периодической системы: LiОН, NaОН, КОН, Са(ОН) 2 и др. При переходе вниз по подгруппе по мере усиления металлических свойств элемента сила гидроксидов возрастает. Растворимые гидроксиды главной подгруппы I группы элементов относят к щелочам.
Щелочами называют растворимые в воде основания. К ним относят также гидроксиды элементов главной подгруппы II группы (щелочно-земельные металлы) и гидроксид аммония (водный раствор аммиака). Иногда щелочами считают те гидроксиды, которые в водном растворе создают высокую концентрацию гидроксид-ионов. В устаревшей литературе вы можете встретить в числе щелочей карбонаты калия К 2 СО 3 (поташ) и натрия Na 2 CO 3 (сода), гидрокарбонат натрия NaHCO 3 (питьевая сода), буру Na 2 B 4 O 7 , гидросульфиды натрия NaHS и калия KHS и др.
Гидроксид кальция Са(ОН) 2 как сильный электролит диссоциирует в одну ступень:
Са(ОН) 2 = Са 2+ + 2ОН – .
3 . Почти все соли. Соль, если это сильный электролит, диссоциирует в одну ступень, например хлорид железа:
FeCl 3 = Fe 3+ + 3Cl – .
В случае водных растворов к слабым электролитам ( < 3%) относят перечисленные ниже соединения.
1 . Вода H 2 O – важнейший электролит.
2
. Некоторые неорганические и почти
все органические кислоты: H 2 S
(сероводородная), H 2 SO 3 (сернистая), H 2 CO 3
(угольная), HCN (циановодородная), Н 3 РО 4
(фосфорная, ортофосфорная), H 2 SiO 3
(кремниевая), H 3 BO 3 (борная, ортоборная),
СН 3 СООН (уксусная) и др.
Заметим, что угольная кислота в формуле H 2 CO 3
не существует. При растворении углекислого газа
СО 2 в воде образуется его гидрат СО 2 Н 2 О,
который мы для удобства расчетов записываем
формулой H 2 CO 3 , и уравнение реакции
диссоциации выглядит так:
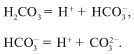
Диссоциация слабой угольной кислоты проходит в
две ступени. Образующийся гидрокарбонат-ион также ведет себя
как слабый электролит.
Точно так же ступенчато диссоциируют и другие
многоосновные кислоты: Н 3 РО 4
(фосфорная), H 2 SiO 3 (кремниевая), H 3 BO 3
(борная). В водном растворе диссоциация
практически проходит лишь по первой ступени. Как
осуществить диссоциацию по последней ступени?
3
. Гидроксиды многих элементов, например
Аl(OH) 3 , Cu(OH) 2 , Fe(OH) 2 , Fe(OH) 3 и др.
Все эти гидроксиды диссоциируют в водном
растворе ступенчато, например гидроксид железа
Fe(OH) 3:
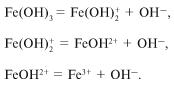
В водном растворе диссоциация проходит
практически только по первой ступени. Как
сместить равновесие в сторону образования ионов
Fe 3+ ?
Осно"вные свойства гидроксидов одного и того же
элемента усиливаются с уменьшением валентности
элемента. Так, осно"вные свойства дигидроксида
железа Fe(OH) 2 выражены сильнее, чем у
тригидроксида Fe(OH) 3 . Это утверждение
равносильно тому, что кислотные свойства Fe(OH) 3
проявляются сильнее, чем у Fe(OH) 2 .
4
. Гидроксид аммония NH 4 OH.
При растворении газообразного аммиака NH 3 в
воде получается раствор, который очень слабо
проводит электрический ток и имеет
горько-мыльный вкус. Среда раствора осно"вная,
или щелочная. Объясняется такое поведение
аммиака следующим образом. При растворении
аммиака в воде образуется гидрат аммиака NH 3 Н 2 О,
которому условно мы приписываем формулу
несуществующего гидроксида аммония NH 4 OH,
считая, что это соединение диссоциирует с
образованием иона аммония и гидроксид-иона ОН – :
NH 4 OH = + ОН – .
5 . Некоторые соли: хлорид цинка ZnCl 2 , тиоцианат железа Fe(NСS) 3 , цианид ртути Hg(CN) 2 и др. Эти соли диссоциируют ступенчато.
К электролитам средней силы некоторые относят фосфорную кислоту Н 3 РО 4 . Мы будем считать фосфорную кислоту слабым электролитом и записывать три ступени ее диссоциации. Серная кислота в концентрированных растворах ведет себя как электролит средней силы, а в очень концентрированных растворах – как слабый электролит. Мы далее будем считать серную кислоту сильным электролитом и записывать уравнение ее диссоциации в одну ступень.
Теорию электролитической диссоциации предложил шведский ученый С. Аррениус в 1887 году.
Электролитическая диссоциация - это распад молекул электролита с образованием в растворе положительно заряженных (катионов) и отрицательно заряженных (анионов) ионов.
Например, уксусная кислота диссоциирует так в водном растворе:
CH 3 COOH⇄H + +CH 3 COO - .
Диссоциация относиться к обратимым процессам. Но различные электролиты диссоциируют по-разному. Степень зависит от природы электролита, его концентрации, природы растворителя, внешних условий (температуры, давления).
Степень диссоциации α - отношение числа молекул, распавшихся на ионы, к общему числу молекул:
α=v´(x)/v(x).
Степень может варьироваться от 0 до 1 (от отсутствия диссоциации до ее полного завершения). Обозначается в процентах. Определяется экспериментальным путем. При диссоциации электролита происходит увеличение числа частиц в растворе. Степень диссоциации показывает силу электролита.
Различают сильные и слабые электролиты .
Сильные электролиты - это те электролиты, степень диссоциации которой превышает 30%.
Электролиты средней силы - это те, степень диссоциации которой делит в пределах от 3% до 30%.
Слабые электролиты - степень диссоциации в водном 0,1 М растворе меньше 3%.
Примеры слабых и сильных электролитов.
Сильные электролиты в разбавленных растворах нацело распадаются на ионы, т.е. α = 1. Но эксперименты показывают, что диссоциация не может быть равна 1, она имеет приближенное значение, но не равна 1. Это не истинная диссоциация, а кажущаяся.
Например, пусть у некоторого соединения α = 0,7. Т.е. по теории Аррениуса в растворе «плавает» 30% непродиссоцииовавших молекул. А 70% образовали свободные ионы. А электролстатическая теория дает другое определение этому понятию: если α = 0,7, то все молекулы диссоциированы на ионы, но ионы свободны лишь на 70%, а оставшиеся 30% - связаны электростатическими взаимодействиями.
Кажущаяся степень диссоциации.
Степень диссоциации зависит не только от природы растворителя и растворяемого вещества, но и от концентрации раствора и температуры.
Уравнение диссоциации можно представить в следующем виде:
AK ⇄ A- + K + .
И степень диссоциации можно выразить так:

С увеличением концентрации раствора степень диссоциации электролита падает. Т.е. значения степени для конкретного электролита не является величиной постоянной.
Так как диссоциация - процесс обратимый, то уравнения скоростей реакции можно записать следующим образом:

Если диссоциация равновесна, то скорости равны и в результате получаем константу равновесия (константу диссоциации):

К зависит от природы растворителя и от температуры, но не зависит от концентрации растворов. Из уравнения видно, что чем больше недиссоциированных молекул, тем меньше величина константы диссоциации электролита.
Многоосновные кислоты диссоциируют ступенчато, и каждая ступень имеет свое значение константы диссоциации.
Если диссоциирует многоосновная кислота, то легче всего отщепляется первый протон, а при возрастании заряда аниона, притяжение возрастает, и поэтому протон отщепляется намного труднее. Например,

Константы диссоциации ортофосфорной кислоты на каждой ступени должны сильно различаться:
I - стадия:

II - стадия:

III - стадия:

На первой ступени ортофосфорная кислота - кислота средней силы, а 2ой - слабая, на 3ей - очень слабая.
Примеры констант равновесия для некоторых растворов электролитов.

Рассмотрим пример:
Если в раствор, в котором содержатся ионы серебра внести металлическую медь, то в момент равновесия, концентрация ионов меди должна быть больше, чем концентрация серебра.
Но у константы низкое значение:
AgCl⇄Ag + +Cl - .
Что говорит о том, что к моменту достижения равновесия растворилось очень мало хлорида серебра.


Концентрация металлической меди и серебра введены в константу равновесия.
Ионное произведение воды.
В приведенной таблице есть данные:
![]()
Эту константу называют ионным произведением воды , которое зависит только от температуры. Согласно диссоциации на 1 ион Н + приходится один гидроксид-ион. В чистой воде концентрация этих ионов одинакова: [H + ] = [OH - ].
Отсюда, [H + ] = [OH - ] = = 10-7 моль/л.
Если добавить в воду постороннее вещество, например, хлороводородную кислоту, то концентрация ионов водорода возрастет, но ионное произведение воды от концентрации не зависит.
А если добавить щелочь, то повысится концентрация ионов, а количество водорода понизится.
Концентрация и взаимосвязаны: чем больше одна величина, тем меньше другая.
Кислотность раствора (рН).
Кислотность растворов обычно выражается концентрацией ионов Н + .
В кислых средах рН
<10 -7 моль/л, в нейтральных - рН
= 10 -7 моль/л, в щелочных - рН
> 10 -7 моль/л.
Кислотность раствора выражают через отрицательный логарифм концентрации ионов водорода, называя ее рН
.
рН = - lg [ H + ].
Взаимосвязь между константой и степенью диссоциации.
Рассмотрим пример диссоциации уксусной кислоты:
Найдем константу:

Молярная концентрация С=1/ V , подставим в уравнение и получим:

Эти уравнения являются законом разведения В. Оствальда , согласно которому константа диссоциации электролита не зависит от разведения растовра.
Измерение степени диссоциации различных электролитов показало, что отдельные электролиты при одинаковой нормальной концентрации растворов диссоциируют на ионы весьма различно.
Особенно велика разница в значениях степени диссоциации кислот. Например, азотная и соляная кислоты в 0,1 н. растворах почти полностью распадаются на ионы; угольная же, синильная и другие кислоты диссоциируют при тех же условиях лишь в не-знaчитeльнoй степени.
Из растворимых в воде оснований (щелочей) слабо диссоциирующим является гидрат окиси аммония, остальные щелочи хорошо диссоциируют. Все соли, за небольшим исключением, также хорошо диссоциируют на ионы.
Различие в значениях степени диссоциации отдельных кислот обусловливается характером валентной связи между атомами, образующими их молекулы. Чем более полярна связь между водородом и остальной частью молекулы, тем легче отщепляется , тем сильнее будет диссоциировать кислота.
Электролиты, хорошо диссоциирующие на ионы, получили название сильных электролитов, в отличие от слабых электролитов, образующих в водных растворах лишь незначительное число ионов. Растворы сильных электролитов сохраняют высокую электропроводность даже при очень больших концентрациях. Наоборот, электропроводность растворов слабых электролитов быстро падает с увеличением концентрации. к сильным электролитам относятся такие кислоты, как соляная, азотная, серная и некоторые другие, затем щелочи (кроме NH 4 OH) и почти все соли.
Многоооновные кислоты и многокислотные основания диссоциируют ступенчато. Так, например, молекулы серной кислоты в первую очередь диссоциируют по уравнению
H 2 SO 4 ⇄ H + HSO 4 ‘
или точнее:
H 2 SO 4 + H 2 O ⇄ H 3 O + HSO 4 ‘
Отщепление второго иона водорода по уравнению
HSO 4 ‘ ⇄ H + SO 4 »
или
HSO 4 ‘ + H 2 O ⇄ H 3 O + SO 4 »
идет уже значительно труднее, так как ему приходится преодолевать притяжение со стороны двухзарядного иона SO 4 », который, конечно, притягивает к себе ион водорода сильнее, чем однозарядный ион HSO 4 ‘. Поэтому вторая ступень диссоциации или, как говорят, вторичная диссоциация происходит в гораздо меньшей степени, чем первичная, и в обычных растворах серной кислоты содержится лишь небольшое число ионов SO 4 »
Фосфорная кислота Н 3 РО 4 диссоциирует в три ступени:
H 3 PO 4 ⇄ H + H 2 PO 4 ‘
H 2 PO 4 ⇄ H + HPO 4 »
HPO 4 » ⇄ H + PO 4 »’
Молекулы Н 3 РO 4 сильно диссоциируют на ионы Н и Н 2 РО 4 ‘. Ионы H 2 PO 4 ‘ ведут себя, как более слабая кислота, и диссоциируют на H и HPO 4 » в меньшей степени. Ионы же НРО 4 » диссоциируют, как очень слабая кислота, и почти не дают ионов Н
и PO 4 »’
Основания, содержащие более одной гидроксильной группы в молекуле, тоже диссоциируют ступенчато. Например:
Ва(ОН) 2 ⇄ ВаОН + ОН’
ВаОН ⇄ Ва + ОН’
Что касается солей, нормальные соли всегда диссоциируют на ионы металлов и кислотных остатков. Например:
СаСl 2 ⇄ Сa + 2Сl’ Na 2 SO 4 ⇄ 2Na + SO 4 »
Кислые соли, подобно многоосновным кислотам, диссоциируют ступенчато. Например:
NaHCO 3 ⇄ Na + НСО 3 ‘
HCO 3 ‘ ⇄ H + CO 3 »
Однако по второй ступени очень мала, так что раствор кислой соли содержит лишь незначительное число ионов водорода.
Основные соли диссоциируют на ионы основных и кислотных остатков. Например:
Fe(OH)Cl 2 ⇄ FeOH + 2Сl»
Вторичной диссоциации ионов основных остатков на ионы металла и гидроксила почти не происходит.
В табл. 11 приведены числовые значения степени диссоциации некоторых кислот, оснований и солей в 0, 1 н. растворах.
С увеличением концентрации уменьшается. Поэтому в очень концентрированных растворах даже сильные кислоты диссоциированы сравнительно слабо. Для
Таблица 11
Кислот, оснований и солей в 0,1 н. растворах при 18°
| Электролит | Формула | Степень диссоциаци и в % |
| Кислоты | ||
| Соляная | HCl | 92 |
| Бромистоводородная | НВr | 92 |
| Йодистоводородная | HJ | . 92 |
| Азотная | HNO 3 | 92 |
| Серная | H 2 SO 4 | 58 |
| Сернистая | H 2 SO 3 | 34 |
| Фосфорная | H 3 PO 4 | 27 |
| Фтористоводородная | HF | 8,5 |
| Уксусная | CH 3 COOH | 1,3 |
| Уголная | H 2 CO 3 | 0,17 |
| Сероводородная | H 2 S | 0,07 |
| Синильная | HCN | 0,01 |
| Борная | H 3 BO 3 | 0,01 |
| Основания | ||
| Гидроксид бария | Ва (OH) 2 | 92 |
| Едкое кали | кон | 89 |
| Едкий натр | NaON | 84 |
| Гидроксид аммония | NH 4 OH | 1,3 |
| Соли | ||
| Хлористый | КСl | 86 |
| Хлористый аммоний | NH4Cl | 85 |
| Хлористый | NaCl | 84 |
| Азотнокислый | KNO 3 | 83 |
| AgNO 3 | 81 | |
| Уксуснокислый | NaCH 3 COO | 79 |
| Хлористый | ZnCl 2 | 73 |
| Сернокислый | Na 2 SO 4 | 69 |
| Сернокислый | ZnSO 4 | 40 |
| Сернокислая |
Которые находятся в динамическом равновесии с недиссоциированными молекулами. К слабым электролитам относится большинство органических кислот и многие органические основания в водных и неводных растворах.
Слабыми электролитами являются:
- почти все органические кислоты и вода;
- некоторые неорганические кислоты: HF, HClO, HClO 2 , HNO 2 , HCN, H 2 S, HBrO, H 3 PO 4 ,H 2 CO 3 , H 2 SiO 3 , H 2 SO 3 и др.;
- некоторые малорастворимые гидроксиды металлов: Fe(OH) 3 , Zn(OH) 2 и др.; а также гидроксид аммония NH 4 OH.
Литература
- М. И. Равич-Шербо. В. В. Новиков «Физическая и коллоидная Химия» М: Высшая школа, 1975
Wikimedia Foundation . 2010 .
Смотреть что такое "Слабые электролиты" в других словарях:
слабые электролиты - – электролиты, незначительно диссоциирующие в водных растворах на ионы. Процесс диссоциации слабых электролитов обратим и подчиняется закону действующих масс. Общая химия: учебник / А. В. Жолнин … Химические термины
Вещества, обладающие ионной проводимостью; их называют проводниками второго рода прохождение тока через них сопровождается переносом вещества. К электролитам относятся расплавы солей, оксидов или гидроксидов, а также (что встречается значительно… … Энциклопедия Кольера
В широком смысле жидкие или твёрдые в ва и системы, в к рых присутствуют в заметной концентрации ионы, обусловливающие прохождение по ним электрич. тока (ионную проводимость); в узком смысле в ва, распадающиеся в р ре на ионы. При растворении Э.… … Физическая энциклопедия
Электролиты - жидкие или твердые вещества, в которых в результате электролитической диссоциации образуются в сколько нибудь заметной концентрации ионы, обусловливающие прохождение постоянного электрического тока. Электролиты в растворах… … Энциклопедический словарь по металлургии
В ва, в к рых в заметной концентрации присутствуют ионы, обусловливающие прохождение электрич. тока (ионную проводимость). Э. также наз. проводниками второго рода. В узком смысле слова Э. в ва, молекулы к рых в р ре вследствие электролитической… … Химическая энциклопедия
- (от Электро... и греч. lytos разлагаемый, растворимый) жидкие или твёрдые вещества и системы, в которых присутствуют в сколько нибудь заметной концентрации ионы, обусловливающие прохождение электрического тока. В узком смысле Э.… … Большая советская энциклопедия
У этого термина существуют и другие значения, см. Диссоциация. Электролитическая диссоциация процесс распада электролита на ионы при его растворении или плавлении. Содержание 1 Диссоциация в растворах 2 … Википедия
Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
Электролит химический термин, обозначающий вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы. Примерами электролитов могут служить кислоты, соли и основания. Электролиты проводники второго рода,… … Википедия
Гидролиз солей
Гидролизом называют реакции взаимодействия вещества с водой, приводящие к образованию слабых электролитов (кислот, оснований, кислых или основных солей). Результат гидролиза можно расценивать как нарушение равновесия диссоциации воды. Гидролизу подвержены соединения различных классов, но наиболее важным случаем является гидролиз солей. Соли, как правило, - сильные электролиты, которые подвергаются полной диссоциации на ионы и могут взаимодействовать с ионами воды.
Важнейшие случаи гидролиза солей :
1. Соль образована сильным основанием и сильной кислотой. Например: NaCl – соль образованная сильным основанием NaOH и сильной кислотой HCl;
NaCl + HOH ↔ NaOH + HCl – молекулярное уравнение;
Na + + Cl - + HOH ↔ Na + + OH - + H + + Cl - – полное ионное уравнение;
HOH ↔ OH - + H + – сокращенное ионное уравнение.
Как видно из сокращенного ионного уравнения соль образованная сильным основанием и сильной кислотой, с водой не взаимодействует, т. е. не подвергается гидролизу, и среда при этом остается нейтральной.
2. Соль образована сильным основанием и слабой кислотой. Например: NaNO 2 – соль, образованная сильным основанием NaOH и слабой кислотой HNO 2 , которая практически не диссоциирует на ионы.
NaNO 2 + HOH ↔ NaOH + HNO 2 ;
Na + + NO 2 - + HOH ↔ Na + + OH - + HNO 2 ;
NO 2 - + HOH ↔ OH - + HNO 2 .
В этом случае соль подвергается гидролизу, причем гидролиз идет по аниону, а катион в процессе гидролиза практически не участвует. Так как в результате гидролиза образуется щелочь, то в растворе находится избыток анионов OH - . Раствор такой соли приобретает щелочную среду, т.е. рН > 7.
I ступень Na 2 СO 3 + HOH ↔ NaOH + NaHCO 3 ;
CO 3 2- + HOH ↔ OH - + HCO 3 - ;
II ступень NaHСO 3 + HOH ↔ NaOH + H 2 CO 3 ;
HCO 3 - + HOH ↔ OH - + H 2 CO 3 .
При стандартных условиях и умеренном разбавлении раствора гидролиз солей протекает только по первой ступени. Вторая - подавляется продуктами, которые образуются на первой ступени. Накопление ионов OH - влечет за собой смещение равновесия влево.
3. Соль образована слабым основанием и сильной кислотой. Например: NH 4 NO 3 – соль, образованная слабым основанием NH 4 OH и сильной кислотой HNO 3 .
NH 4 NO 3 + HOH ↔ NH 4 OH + HNO 3 ;
NH 4 + + HOH ↔ H + + NH 4 OH.
В этом случае соль подвергается гидролизу, причем гидролиз идет по катиону, а анион в процессе гидролиза практически не участвует. Раствор такой соли приобретает кислую среду, т.е. рН < 7.
Как и в предыдущем случае, соли многозарядных ионов гидролизуются по стадиям, хотя вторая стадия также подавляется.
I ступень Mg(NO 3) 2 + HOH ↔ MgOHNO 3 + HNO 3 ;
Mg 2+ + HOH ↔ MgOH + + H + ;
II ступень MgOHNO 3 + HOH ↔ Mg(OH) 2 + HNO 3 ;
MgOH + + HOH ↔ Mg(OH) 2 + H + .
4. Соль образована слабым основанием и слабой кислотой. Например: NH 4 CN – соль, образованная слабым основанием NH 4 OH и слабой кислотой HCN.
NH 4 CN + HOH ↔ NH 4 OH + HCN ;
NH 4 + + CN - + HOH ↔ NH 4 OH + HCN.
В этом случае в гидролизе участвуют и катионы и анионы. Они связывают и водородные катионы, и гидроксо-анионы воды, образуя слабые электролиты (слабые кислоты и слабые основания). Реакция раствора таких солей может быть либо слабокислой (если основание, образовавшееся в результате гидролиза, является более слабым, чем кислота), либо слабощелочной (если основание окажется более сильным, чем кислота), либо будет нейтральной (если основание и кислота проявляют одинаковую силу).
При гидролизе соли многозарядных ионов I стадия не подавляет последующие, и гидролиз таких солей протекает полностью даже при комнатной температуре.
I ступень (NH 4) 2 S + HOH ↔ NH 4 OH + NH 4 HS ;
2NH 4 + + S 2- + HOH ↔ NH 4 OH + NH 4 + + HS - ;
II ступень NH 4 HS + HOH ↔ NH 4 OH + H 2 S ;
NH 4 + + HS - + HOH ↔ NH 4 OH + H 2 S.
Похожие статьи
-
Великая отечественная война Окончательное снятие блокады Ленинграда
Великая Отечественная война - война СССР с Германией и ее союзниками в – годах и с Японией в 1945 году; составная часть Второй мировой войны . С точки зрения руководства нацистской Германии, война с СССР была неизбежна. Коммунистический...
-
Под знаком зодиака Дева, были рождены прославленные люди
Действительное описание — даты календаря 31 августа.Астрологический символ людей родившихся в день 31.08.90 года ›››› Дева (с 22 августа по 23 сентября).Восточный календарь, 1990 год = ››› Белой Металлической Лошади.Стихия знака гороскопа...
-
КВР: расшифровка. Что означает КВР? Какие квр и косгу использовать для госзакупок Квр 243 расшифровка в году
Комбинация КВР - КОСГУ имеет закрытый перечень. Использование иных сочетаний может стать причиной нарушения методологии учета. А значит, и штрафных санкций. Узнайте, как без ошибок увязать КВР и КОСГУ. КВР и КОСГУ по страховым взносам...
-
Значение слова посредник Кто такой посредник
Слово «посредник», наверное, слышали все. Здесь буду говорить о посредниках в торговле. Если вам больше 15 лет, то наверняка вы знаете, что очень редко товары доходят до нас «напрямую» с производства. В 90% случаев между производителем и...
-
Русский консерватизм первой четверти XIX века Идеология консерватизма в 19 веке
Консерватизм возник как непосредственная реак-ция на Великую французскую революцию. В Велико-британии его основоположником стал Эдмунд Бёрк (1729-1797), известный политический деятель и один из самых оригинальных мыслителей своего...
-
Вольфганг Шойбле (Wolfgang Schaeuble) - это Предложение о создании конкурента МВФ
(Wolfgang Schäuble), занимавший в уходящем правительстве пост министра финансов. За его кандидатуру, предложенную главой крупнейшей фракции Христианско-демократического и Христианско-социального союзов (ХДС/ХСС) Фолькером Каудером (Volker...
